موفقیتی بیسابقه در ویرایش مستقیم ژنهای سلولهای بنیادی

پژوهشی جدید تحت هدایت ایمی ویجرز از دانشگاه هاروارد نشان داده است که میتوان ماشین ویرایش ژن را مستقیما در محل زندگی سلولهای بنیادی به آنها تحویل داد و دیگر لازم نیست این کار در ظرف آزمایشگاهی انجام شود. یافتههای این پژوهش که در مجلهی Cell Reports گزارش شده است، دارای تلویحات مهمی برای پژوهشهای بیوتکنولوژی و توسعهی درمانهایی برای بیماریهای ژنتیکی است. ویگرز میگوید:
اگر شما بخواهید یک ژنوم را تغییر دهید تا یک جهش مسبب بیماری را تصحیح کنید، باید آن را در سلولهای بنیادی مربوطه اصلاح کنید. اگر سلولهای بنیادی را تغییر ندهید، هر سلولی که اصلاح کنید، ممکن است درنهایت با سلولهای دارای جهش جایگزین شود. اگر سلولهای بنیادی را اصلاح کنید، آنها سلولهای سالمی حاصل خواهند کرد که میتواند درنهایت جایگزین سلولهای بیمار شود.
اما اصلاح سلولهای بنیادی سختتر از چیزی است که بهنظر میرسد. روال فعلی این کار این است که باید سلولهای بنیادی استخراج شوند، زنده و سالم نگاه داشته شده، ازلحاظ ژنتیکی تغییر داده شوند و درنهایت مجددا وارد بدن بیمار شوند. این فرایند برای سلولها تخریبکننده است و ممکن است پیوند این سلولها به بیمار موفقیتآمیز نباشد. ویگرز میگوید:
هرکدام از سلولهای بنیادی در محل خاص خود زندگی میکند؛ در مناطق بهخوبی محافظت شده و دشوار ازنظر دسترسی مانند مغز استخوان. وقتی سلولهای بنیادی را از بدن خارج میکنید، آنها را از محیط بسیار پیچیدهای که از آنها محافظت کرده و آنها را تغذیه میکنند، جدا میکنید و این نوعی شوک برای آنها خواهد بود. دور کردن سلولها از این محیط موجب تغییر آنها میشود. پیوند سلولها نیز موجب تغییر آنها میشود. چیزی که ما بهدنبال آن بودیم، ایجاد تغییر ژنتیکی در این سلولها بدون نیاز به این مراحل بود بهطوریکه تعاملات تنظیمی بین سلولها حفظ شود.
انتقال بهوسیلهی ویروس
گروه ویگرز از ویروس وابسته به آدنو (AAV) که سلولهای انسان (و موش) را عفونی میکند ولی موجب بروز بیماری نمیشود بهعنوان وسیلهی انتقال استفاده کردند. پژوهشگران براساس کار قبلی خود روی موشهای مبتلا به دیستروفی ماهیچهای دوشن، پکیجهای AAV مختلفی را برای تحویل محمولهی ویرایش ژن به چندین نوع مختلف از سلولهای پوست، خون، سلولهای بنیادی عضله و سلولهای پروژنیتور طراحی کردند. جیل گلدستین، پژوهشگر دیگر مقاله میگوید:
این یک همکاری حقیقی بین آزمایشگاههای مختلف بود که هرکدام در زمینهی عضو خاصی تخصص داشتند. ما آزمایشها، تجزیهوتحلیلها و مقایسات مختلفی روی هر کدام از اعضای مورد آزمایش انجام دادیم. ما قادر نبودیم این کار را بهتنهایی پیش ببریم. این کار نیاز به همکاری گستردهای داشت و طی رویکرد سرگرمکنندهای انجام شد.
پژوهشگران برای آزمون اینکه آیا میتوانند کمپلکسهای AAV را به سیستم زنده تحویل دهند، از موشهایی استفاده کردند که مانند یک سیستم حملونقل گزارشگر عمل میکردند. آنها دارای یک ژن گزارشگر بودند که بهطور طبیعی غیرفعال بود ولی میتوانست با ویرایش ژن فعال شود. زمانیکه این ژن فعال میشد، بهعلت رنگ فلورسنت قرمز سلول به رنگ قرمز درمیآمد.
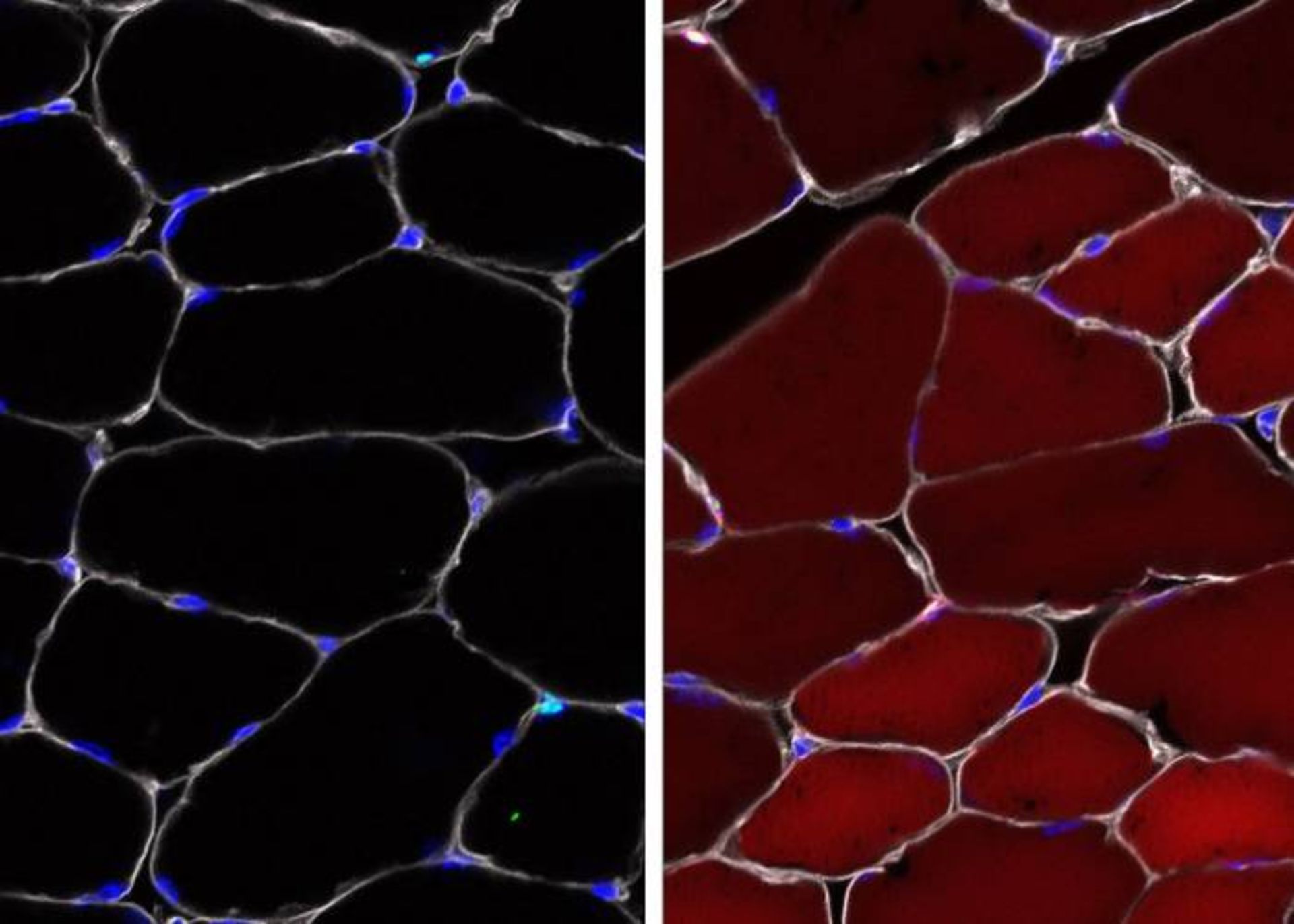
در ماهیچهی اسکلتی، تا ۶۰ درصد از سلولهای بنیادی به رنگ قرمز فلورسنت درآمدند. در سلولهای پوستی تا ۲۷ درصد از سلولها قرمز شدند. همچنین تا ۳۸ درصد از سلولهای بنیادی مغز استخوان (که خون را میسازند) تغییر پیدا کردند. این ممکن است بهنظر کم بیاید اما خون با چنان سرعتی در حال حرکت و تغییر است که در برخی از موارد حتی یک سلول بنیادی سالم نیز میتواند برای نجات از یک نقص کافی باشد. شریف تابعبردبار پژوهشگر مطالعه میگوید:
تاکنون ایدهی تحویل ژنهای سالم به سلولهای بنیادی با استفاده از AAV عملی نبوده است زیرا این سلولها در سیستمهای زنده با سرعت زیادی تقسیم میشوند و ژنهای تحویل داده شده سریعا رقیق میشوند. مطالعهی ما نشان میدهد که ما میتوانیم بهطور دائمی ژنوم سلولهای بنیادی و بنابراین ژنوم سلولهای حاصل از آنها را در محیط آناتومیکی طبیعیشان تغییر دهیم. ظرفیت زیادی برای استفاده از این رویکرد و توسعهی درمانهای دائمی برای انواع مختلف بیماریهای ژنتیکی وجود دارد. اینها شامل اشکال مختلف دیستروفی ماهیچه میشوند که در آن تخریب بافت عامل بسیار مهمی است.
یاچیه هسو پژوهشگر دیگر این مطالعه میگوید:
ما به پوست موشهای مورد آزمایش نگاه کردیم و خوشحال شدیم که دیدیم بسیاری از سلولهای پوست نیز بهطور موفقیتآمیزی ویرایش شده بودند. اینها شامل سلولهایی بودند که به آدیپوسایتهای پوستی تبدیل میشوند و نیز سلولهایی که به تنظیم دیگر سلولهای بنیادی موجود در پوست کمک میکنند. ما همیشه نیاز به ابزاری داشتهایم که به ما اجازه دهد سلولهای پوستی را در بدن موجود زنده با سرعت دستکاری کنیم، بنابراین برای ما این همچون خوابی است که به واقعیت تبدیل شده است.
تحویل مستقیم ژندرمانی به یک سیستم زنده، مانعی برای تلاش شرکتهای بیوتکنولوژی درجهت توسعهی درمانهایی برای بیماریهایی نظیر آتروفی عضلانی نخاعی بوده است. ویگرز میگوید:
این مطالعه دو پیامد مهم دارد. نخست اینکه این رویکرد نحوهی مطالعهی سلولهای بنیادی در بدن را تغییر میدهد. رویکرد AAV بررسی سریع اهمیت ژنهای مختلف سلولهای بنیادی را در محیط طبیعی امکانپذیر میکند. بهعلت اینکه این سیستم تحویل کاملا قاطع است، میتواند همچنین برای هدف قرار دادن ژنهایی که بافتهای مختلف را تختتاثیر قرار میدهند، استفاده شود. دوم، این یک امر مهم در جهت توسعهی ژندرمانیهای مؤثر است. رویکردی که ما توسعه دادهایم بر تمام مشکلاتی که شما با خارج کردن سولهای بنیادی از بدن با آن مواجه میشوید، غلبه میکند و به شما اجازه میدهد که بهطور دائمی یک ژنوم را تصحیح کنید. از آنجایی که در حال حاضر در کلینیکها از AVV برای اهداف ژندرمانی استفاده میشود، سرعت پیشرفت رویکرد حاضر زیاد خواهد بود.
نظرات