سلولهایی که میتوانند به شما ایمنی فوقالعاده بدهند
در اکتبر ۲۰۲۰، تیمی از ویروسشناسان در دانشگاه راکفلر در نیویورک پروژهی یک سالهای را آغاز کردند تا پیشبینی کنند که چه گونههای خطرناکی از کووید ۱۹ ممکن است در آینده ظاهر شود.
درحالیکه کابوس گونههای جدید هنوز ذهن رهبران سیاسی و شهروندان را به خود مشغول نکرده بود، دانشمندان میدانستند که کووید ۱۹ به احتمال زیاد به روشهایی جهش پیدا خواهد کرد که آن را مسریتر و بیماریزاتر کند.
هدف دانشمندان راکفلر ایجاد نسخهای مصنوعی از پروتئین اسپایک کووید ۱۹ بود (پروتئینی که ویروس از آن برای نفوذ به داخل سلولهای ما استفاده میکند) که بتواند از تمام آنتیبادیهای محافظی که در خون بازماندگان کووید ۱۹ شناخته شده بود، فرار کند.
پژوهشگران طی ۱۲ ماه بعدی، با ترکیبهای مختلف جهشها روی سطح پروتئین اسپایک کار کردند تا مجموعهای از ۲۰ جهش را پیدا کردند که به نظر میرسید ویروس را بهطور خاص در برابر هر چیزی که سیستم ایمنی میتواند به سمت آن پرتاب کند، مقاوم میکند. آنها برای آزمایش این مجموعه جهش، آن را وارد «ویروس نوع کاذب» کردند. ویروس نوع کاذب ویروسی است که به گونهای مهندسی شده که ماده ژنتیکی کافی برای تکثیر ندارد و به دانشمندان اجازه میدهد که آن را تغییر دهند و بدون خطر فرار، رفتار آن را درک کنند.
در ابتدا همه چیز طبق انتظار پیش رفت. وقتی ویروسشناسان ویروس مهندسیشدهی خود را در معرض نمونههای خون گرفتهشده از افرادی که یا از کووید ۱۹ بهبود پیدا کرده بودند، یا در برابر این بیماری واکسینه شده بودند، قرار دادند، ویروس بهطرز ماهرانهای از تمام آنتیبادیهای آنها، فرار کرد.
اما پس از آن اتفاق شگفتآوری رخ داد. زمانی که پژوهشگران ویروس مهندسیشدهی خود را روی خون افرادی آزمایش کردند که در سال ۲۰۲۰ از کووید ۱۹ بهبود پیدا کرده بودند و چند ماه بعد واکسن زده بودند، آنتیبادیهای آنها قادر بودند که به ویروس متصل شده و آن را بهطور کامل خنثی کنند.
میشل نوسنزویگ، استاد ایمنیشناسی مولکولی در دانشگاه راکفلر و یکی از دانشمندان دخیل در پروژه میگوید: «دیدن آن باورکردنی نبود. یکی از بزرگترین درسهایی که از دنیاگیری یاد گرفتهایم، این است که چگونه پاسخ سیستم ایمنی بسته به اینکه آیا بهطور طبیعی آلوده شدهایم، واکسن زدهایم یا هر دو، متفاوت است.» (البته این بدان معنا نیست که ایده خوبی است که بهطور عمدی آلوده شوید، چراکه هر عفونتی با خطرهایی همراه است).
طی چهار ماه گذشته، یافتههای تیم راکفلر بارها در زندگی واقعی مشاهده شده است. افرادی که از عفونت کووید ۱۹ بهبود پیدا کردهاند و سپس واکسینه شدهاند، به نظر میرسد در برابر گونههای جدید از دلتا گرفته تا اومیکرون مقاومت بیشتری داشته باشند.
ایمنیشناسان نمونههای خون این افراد را گرفتند و دریافتند که آنها دارای نوعی ایمنی فوقالعاده هستند که جامعه علمی آن را ایمنی ترکیبی (هیبرید) مینامد. این افراد نهتنها سطوح بسیار بالایی از آنتیبادیها را تولید میکنند (بسیار بیشتر از کسانی که بهطور کامل واکسینه شدهاند)، بلکه طیف بسیار متنوعتری از آنتیبادیها را تولید میکنند که شانس بیشتری برای پیدا کردن نقاط ضعف ویروس حتی در اشکال بسیار جهشیافته کووید ۱۹ دارند.
سلولهای B اولینبار در دههی ۱۹۶۰ در مرغ کشف شدند.
مطالعه اخیری از دانشمندان در بوستون و آفریقای جنوبی نشان داد، افرادی که پیش از تزریق دو نوبت واکسن و یک دوز تقویتکننده، به یکی از گونههای کووید ۱۹ آلوده شده بودند، دارای ایمنی بیشتری در برابر اومیکرون بودند. اومیکرون نزدیکترین گونه در دنیای واقعی به ویروس مصنوعی راکفلر است. نوسنزویگ میگوید:
زمانی که افرادی که قبلاً دچار کووید ۱۹ شدهاند، با واکسن mRNA واکسینه میشوند، پاسخ آنتیبادی را تولید میکنند که سه برابر افرادی است که بدون اینکه قبلاً دچار عفونت شده باشند، واکسینه شدهاند.
اما دلیل اینکه این افراد چنین پاسخهای قوی را از خود نشان میدهند، مربوط به جنبهای از سیستم ایمنی است که مدتها نادیده گرفته شده بود، یعنی نوعی از سلولهای سفید خون که «سلولهای B خاطره» نامیده میشوند.
برای مدت طولانی، دانش کمی در مورد سلولهای B خاطره و نحوه رفتار آنها داشتیم؛ اما از طریق پژوهشهایی که روی اچآیوی، ابولا و بیماریهای خودایمنی و اکنون کووید ۱۹ انجام شده است، شروع به درک این مسئله کردهایم که سلولهای مذکور چقدر در تعیین پاسخهای ما در برابر عفونتها و واکسنها حیاتی هستند.
از مرغها تا اچ آی وی
در دههی ۱۸۹۰، امیل فون برینگ، فیزیولوژیست آلمانی (مردی که بهخاطر پژوهشهای خود روی درمان کزاز و دیفتری که به موجب آن برنده جایزه نوبل شد، با عنوان ناجی کودکان شناخته میشد)، وجود سلولهایی را پیشنهاد کرد که میتوانستند رویاروییهای گذشته با عفونت خاص را به خاطر بسپارند و زمانی که دوباره در معرض آن قرار میگرفتند، آنتیبادی تولید کنند.
هفتاد سال طول کشید تا ایدههای فونبرینگ اثبات شود. در دههی ۱۹۶۰، ایمنیشناسان دریافتند مرغهایی که بورس (کیسه سینوویال: یکی از ارگانهای ایمنی اصلی در پرندگان) آنها بر اثر تشعشع تخریب شده بود، فاقد سلولهای خاصی بودند که برای تولید آنتیبادی لازم است. این سلولها بهعنوان «سلولهای مشتقشده از بورس» یا «سلولهای B» معروف شدند. تا اواسط دههی ۱۹۷۰، کشف شد که این سلولها در انسانها قبل از مهاجرت به گرههای لنفای یا طحال، در مغز استخوان تشکیل میشوند.
اکنون میدانیم که در طول زندگی، بهطور مداوم در حال تولید سلولهای B جدید هستیم. بدن حدود ۱۰ میلیارد سلول B دارد (اگر آنها را در طول خطی پشت سر هم ردیف کنید، به طول ۱۰۰ زمین فوتبال میرسد) و هر سلول B حاوی گیرندههایی است که آنتیژنهای مختلف موجود روی سطح ویروس را تشخیص میدهند.
این امر اهمیت دارد، زیرا درحالیکه سلولهای B خود به ویروسها متصل نمیشوند، زمانی که تهدیدی را شناسایی کنند، میتوانند به سلولهای پلاسما تبدیل شوند. این سلولهای پلاسما آنتیبادیهایی را تولید میکنند که همان آنتیژن ویروسی را شناسایی میکنند که سلول B اصلی آن را شناسایی میکند. تنوع کم سلولهای B بهمعنای آنتیبادیهای کمتری است که ممکن است بتوانند ویروس را خنثی کنند.
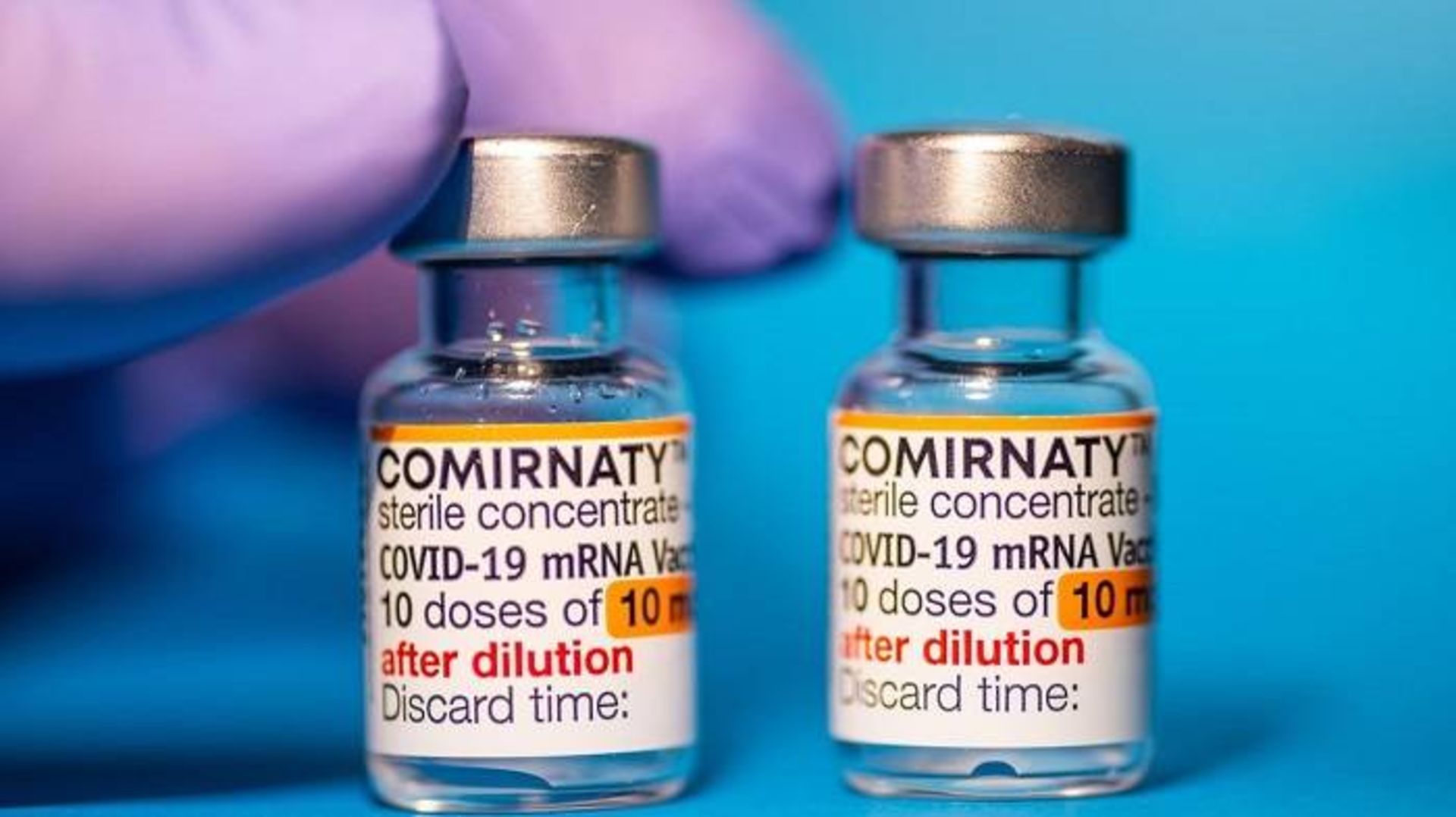
تا به اینجا، شواهد نشان میدهند که واکسنهای mRNA کووید ۱۹ نسبت به انواع دیگر واکسنها موجب پاسخ قویتری از سوی سلولهای B خاطره میشوند.
یکی از موضوعاتی که کووید ۱۹ آن را برای ایمنیشناسان آشکار کرده است، این است که افرادی که دارای تنوع بالاتری از سلولهای B هستند، برای دفع پاتوژن جدید و خصوصاً گونههای جدید کووید ۱۹ بسیار مجهزتر هستند. این مسئله تحت تأثیر سن، شرایط سلامتی و ژنتیک نیز قرار دارد. علی البدی، دانشیار آسیبشناسی و ایمنیشناسی در دانشکده پزشکی دانشگاه واشینگتن میگوید:
هر کسی مجموعه متفاوتی از سلولهای B خواهد داشت که به کمک آنها به هر عفونتی پاسخ میدهد. حتی اگر خواهر و برادرانی داشته باشید، آنها پاسخهای سلول B متفاوتی خواهند داشت.
با افزایش سن، دو اتفاق برای پاسخ سلول B رخ میدهد. اول اینکه بدن شروع به تولید مجموعه کوچکتری از سلولهای B میکند، یعنی احتمال کمتری وجود دارد که آنها گیرندههایی داشته باشند که آنتیژنهای روی ویروس جدیدی را تشخیص دهند. موضوع مهمتر اینکه، بسیج شدن آنها علیه تهدید بیشتر طول میکشد، بنابراین پاتوژنهای کشنده میتوانند قبل از اینکه سیستم ایمنی وارد عمل شود، بر آن غلبه کنند. همین عوامل هستند که موجب میشوند افراد جوانتری که دچار بیماریهای زمینهای هستند، در برابر کووید ۱۹ آسیبپذیرتر باشند.
اما هنگامی که بدن شما با عفونتی مبارزه میکند یا واکسنی را دریافت میکنید، این امر موجب آغاز ترفند ایمنیشناختی هوشمندانهای میشود. برخی از سلولهای B به سلولهای B خاطره تبدیل میشوند که میتوانند برای دههها در جریان خون گردش کنند و آمادهاند تا در صورت برگشت ویروس دوباره فعال شوند و پاسخ آنتیبادی را راهاندازی کنند.
چنین آنتیبادیهایی همچنین در سرکوب عفونتهای مزمنی مانند ویروس اپشتین بار که در بیشتر طول عمر ما در بدن به شکل نهفته باقی میمانند، نقش دارند. به نظر میرسد این ویروسها پس از ضعیف شدن بدن میتوانند دوباره فعال شوند (به نظر میرسد که این اتفاق در بخشی از بیماران دچار کووید طولانی رخ میدهد).
اما تفاوتهای ظریف زیادی در پاسخ سلولهای B خاطره وجود دارد. یکی از مواردی که ایمنیشناسان از مطالعات بازماندگان ابولا آموختهاند، این است که بهنظر میرسد عفونتهای شدید نسبت به واکسنها بهتنهایی، موجب تحریک تعداد بسیار بیشتری از سلولهای B خاطره شوند. نوسنزویگ میگوید:
وقتی عفونت بدی دارید، سلولهای بدن شما مقدار زیادی ویروس تولید میکنند. ویروس در سراسر سیستم تنفسی، بینی، ریهها، مجاری هوایی فوقانی و مخاط وجود دارد. تمام سیستم ایمنی در پاسخ نقش دارد و به تمام عناصر ویروس پاسخ میدهد، بنابراین این امر یکی از دلایل احتمالی است که چرا عفونتهای طبیعی ممکن است موجب حافظه بهتر سیستم ایمنی شوند.
افرادی که علیه کووید ۱۹ واکسینه شدهاند و در معرض ویروس قرار گرفتهاند، ممکن است ایمنی ترکیبی مفیدی داشته باشند. اگرچه، هر عفونتی با خطراتی همراه است.
در طول شش ماه گذشته، نوسنزویگ تفاوتهای ظریف میان عفونت طبیعی ناشی از کووید ۱۹ و واکسیناسیون را مطالعه کرده است. او از طریق جداسازی سلولهای B خاطره از افرادی که در مقاطع زمانی مختلف عفونی یا واکسینه شدهاند، متوجه شد که بهنظر میرسد عفونت طبیعی موجب تولید سلولهای B خاطرهای میشود که بهطور مداوم تکامل پیدا میکنند. این بدان معنا است که آنها آنتیبادیهایی تولید میکنند که با احتمال بیشتری قادر به محافظت در برابر گونههای جدید ویروس هستند. نکته مهمی که ایمنیشناسان به آن پی بردند، این بود که این اثر زمانی که افراد عفونی شده و سپس واکسینه شده باشند، با شدت بیشتری اتفاق میافتد.
اکنون دانشمندان بهدنبال درک این موضوع هستند که آیا میتوانیم رژیمهای واکسن را به گونهای تنظیم کنیم که بهتنهایی بتوانند موجب ایجاد پاسخ ایمنی ترکیبی شوند. موفقیت در انجام این کار میتواند سلاح مهمی در برابر گونههای جدید کووید ۱۹ و دنیاگیریهای آینده در اختیار بشریت قرار دهد.
دنیاگیری بعدی
در سال ۲۰۰۷، گروهی از پژوهشگران دانشگاه بهداشت و علوم اورگن مأموریتی را برای درک این موضوع آغاز کردند که چرا بهنظر میرسد پاسخ ایمنی به برخی از عفونتها یا واکسنها نسبتبه عفونتها و واکسنهای دیگر بادوامتر باشد.
پژوهشگران آنتیبادیهای تولیدشده توسط یک سری از فناوریهای رایج واکسن را مقایسه کردند: واکسن سرخک (که فرم ضعیفشدهای از ویروس کامل را به بدن میرساند)، واکسنهای کزاز و دیفتری (که حاوی آنتیژنهای ویروسی هستند) و آنتیبادیهای تولیدشده توسط پاتوژنهای شایعی مانند ویروس اپشتینبار یا سیتومگالوویروس.
مقاله حاصل نشان داد، نیمهعمر آنتیبادیها بسته به نوع ویروس یا واکسن بهشدت متفاوت است. درحالیکه آنتیبادیهای تولیدشده برای سرکوب سیتومگالوویروس تقریباً بهطور نامحدود در بدن میماندند، پاسخ به کزاز پس از چند سال کاهش پیدا میکرد. جان وری، مدیر مؤسسه ایمنیشناسی در دانشگاه پنسیلوانیا میگوید: «این نتایج به ما نشان داد که برنامهریزی سلولی که موجب ایجاد سلولهای B خاطره میشود، بستهبه ماهیت عفونت یا ایمونوژن بسیار متفاوت است.»
اکنون کووید ۱۹ فرصت منحصربهفردی برای مقایسه فناوریهای مختلف واکسن برای یک ویروس فراهم کرده است تا با مشاهده نحوه پاسخ سلولهای B خاطره در طول زمان درک کنیم که چه چیزی موجب بادوامترین و مؤثرترین پاسخ ایمنی میشود.
تا اینجا، به نظر میرسد که واکسنهای RNA پیامرسان مانند واکسنهایی که توسط فایزر، مدرنا و نوارتیس تولید شده است، بهترین عملکرد را دارند، اگرچه پژوهشگران هنوز در تلاش هستند تا علت دقیق آن را کشف کنند. البدی میگوید: «این واکسنها پاسخ سلول B خاطره قویتری تولید میکنند. اگر آن را بهعنوان مثال با واکسن آنفلوانزا مقایسه کنید، میبینید که پاسخ حداقل ده برابر بیشتر است.»
دانشمندان در حال کار روی نسل جدیدی از واکسنها هستند که میتواند به اندازه عفونتهای جدی ناشی از برخی از ویروسها، سلولهای B خاطره تولید کند.
کشف جالب ایمنی ترکیبی در ماههای اخیر موجب شد دانشمندان رژیمهای مختلف واکسن کووید ۱۹ را تجزیهوتحلیل کنند تا ببینند که آیا ترکیب واکسنهای مختلف میتواند موجب پاسخ ایمنی قوی مشابهی شود.
نوسنزویگ میگوید اولین دادههای محکم در این مورد در سال ۲۰۲۲ به دست خواهد آمد و میتواند به ما در پیدا کردن بهترین روش استفاده از واکسنها و دوزهای تقویتکننده در برابر ویروسهای دیگر از آنفلوانزا گرفته تا اچآیوی کمک کند. او میگوید:
حجم عظیمی از دادههای بالینی و ایمنیشناختی را خواهیم داشت که براساس آن بهترین روشها را پیدا خواهیم کرد. برای مثال، اینکه آیا برای افرادی که آلوده نشدهاند، دادن یک دوز تقویتکننده علاوه بر آنتیبادیهایی که از قبل در گردش هستند، سلولهای B خاطره آنها را تقویت میکند؟ آیا این کار موجب میشود که افراد در مقابله با عفونت بعدی کووید بهتر عمل کنند؟ میتوانیم همهی اینها را در کنار هم قرار دهیم و مثلاً بگوییم: کاری که باید انجام میدادیم، این بود که به همه واکسن mRNA میدادیم. بهترین تعداد دوزهای واکسن این مقدار و بهترین فاصله بین دوزهای این اندازه است.
وری پیشبینی میکند که افزایش درک ما از سلولهای B ازطریق مطالعهی کووید ۱۹ میتواند همچنین مزیتهایی در حوزه ایمنیدرمانی سرطان داشته باشد.
سلولهای B به همان روشی که در برابر ویروس عمل میکنند، آنتیبادیهایی را علیه قسمتهای خاصی از تومورها میسازند. سلولهای B همچنین با اجزای دیگر سیستم ایمنی مانند سلولهای T و سلولهای دندریتیک برای ایجاد محیط مناسبی برای حمله به تومور همکاری میکنند و یکی از اهداف ایمنیدرمانیهای آینده تحریک تعامل میان این سلولها است. وری میگوید: «این تعامل کوچک سه سلولی با نتیجه بهتر برای تمام درمانهای سرطان همراه است. هر وقت این اتفاق میافتد، نتیجه بهتری میگیرید.»
دانستن اینکه چگونه سیستم ایمنی را به بهترین نحو فعال کنیم، همچنین نقش بزرگی در توانمندسازی سیستمهای مراقبتهای بهداشتی برای واکنش سریع و کاهش مرگومیر هنگام وقوع دنیاگیری بعدی دارد. بیشتر دانشمندان بر این باورند که وقوع دنیاگیریهای بعدی اجتنابناپذیر است. نوسنزویگ میگوید: «دفعهی بعدی وجود خواهد داشت. سه ویروس سارس طی ۲۰ سال گذشته ظاهر شدهاند و مشکلات بزرگی ایجاد کردهاند. نمیدانیم پاتوژن بعدی که موجب دنیاگیری میشود چه خواهد بود، اما باید برای آن آماده باشیم.»